அமிலங்கள்/Acids
அமிலம் என்பது சேர்மம், நிரில் கரையும் பொழுது ஹைட்ரஜன் அயனிகளைத் (H) தரவல்லது. அதே போல் காரம் என்பதும் சேர்மம், நீரில் கரையும் பொழுது ஹைட்ராக்சைடு (OH) அயனிகளைத் தரவல்லது. அமிலமும், காரமும் ஒன்றோடொன்று வினைபுரிந்து நடுநிலைவினை விளைபொருளைத் தருகின்றன அதுவே உப்பு ஆகும்.
ஆசிட் என்ற ஆங்கிலச் சொல்' அசிடஸ்' என்ற இலத்தீன் மொழியிலிருந்து பெறப்பட்டது. அதன் பொருள் புளிப்புச்சுவை புளிப்புச் சுவை கொண்ட பொருள்கள் அமிலங்கள் எனப்படும்
1884 ஆம் ஆண்டு ஸ்வீடன் நாட்டு வேதியியலார் ஸ்வான்டே அர்ஹீனியஸ் அமிலங்கள் மற்றும் காரங்களைப் பற்றிய கொள்கையை முன்மொழிந்தார் அர்ஹீனியஸ் கூற்றுப்படி அமிலங்கள் நீரில் கரையும் பொழுது H அயனிகளையோ அல்லது H.O
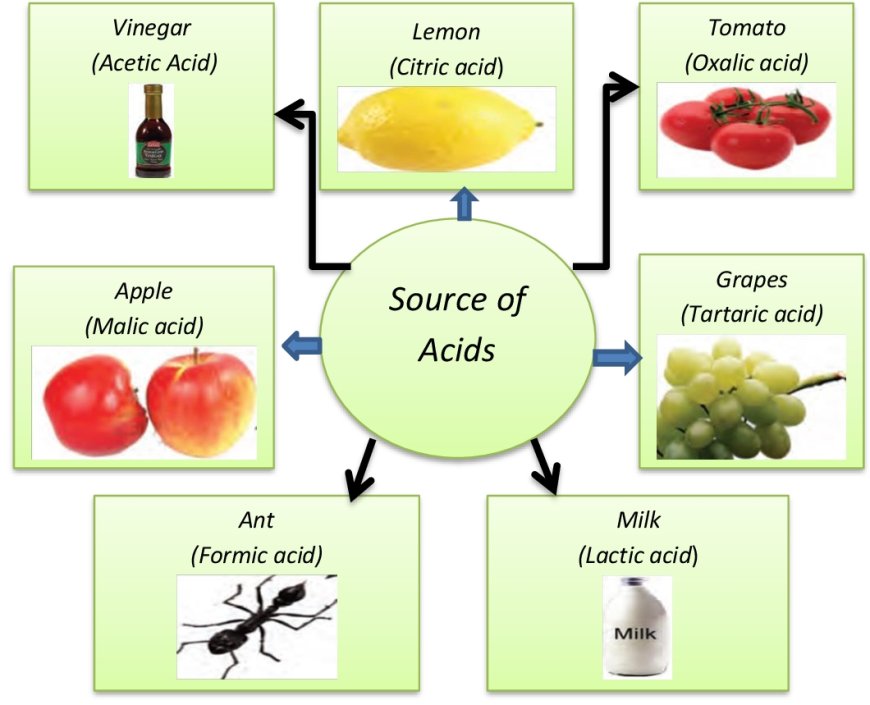
மூலங்கள் - அமிலங்கள்
ஆப்பிள் - மாலிக் அமிலம்
எலுமிச்சை சிட்ரிக் அமிலம்
திராட்சை டார்டாரிக் அமிலம்
தக்காளி - ஆக்ஸாலிக் அமிலம்
வினிகர் அசிட்டிக் அமிலம்
தயிர் லாக்டிக் அமிலம்
ஆரஞ்சு - அஸ்கார்பிக் அமிலம்
தேநீர் டானிக் அமிலம்
வயிற்றில் சுரக்கும் அமிலம் ஹைட்ரோகுளோரிக் அமிலம்
எறும்பு தேனீயின் கொடுக்கு பார்மிக் அமிலம்
* அனைத்து அமிலங்களும் ஒன்று அல்லது அதற்கு மேற்பட்ட ஹைட்ரஜன் அணுக்களைக் கொண்டவை. ஆனால் ஹைட்ரஜன் உள்ள அனைத்துப் பொருள்களும் அமிலங்கள் அல்ல எ.கா. மீத்தேன் (CH) மற்றும் அம்மோனியா (NH,) ஆகியவை ஹைட்ரஜனைக் கொண்டுள்ளன. ஆனால் இவை நீர்த்த கரைசலில் ஹைட்ரஜன்(H*) அயனிகளைத் தராது
* அமிலங்களுக்கு காரத்துவம் என்ற பதத்தைப் பயன்படுத்துகிறோம். இது அறிலுள்ள இடப்பெயர்ச்சி செய்யக்கூடிய ஹைட்ரஜன் அணுக்களின் எண்ணிக்கையைக் குறிப்பதாகும். எகா அசிட்டிக் அமிலத்தில் (CH, COOH) நான்கு ஹைட்ரஜன் அணுக்கள் இருந்தாலும், ஒரே ஒரு ஹைட்ரஜனை மட்டுமே இடப்பெயர்ச்சி செய்ய முடியும். எனவே இது ஒற்றைக் காரத்துவமுடையது.
*வெப்பம் அல்லது கதிர்வீச்சு அல்லது வேருளினை அல்லது மின்னிறக்கத்தால் அயனிகளைப் பிரித்தெடுக்கும் நிலை அயனியாதல் எனப்படும்
அமிலங்களின் பண்புகள்
அ) அமிலங்கள் புளிப்புச் சுவை உடையவை
ஆ) இவற்றின் நீர்த்த கரைசல்கள் மின்சாரத்தைக் கடத்தும். ஏனென்றால், இவை அயனிகளைக் கொண்டுள்ளன.
இ) இவை நீல லிட்மஸ்தாளை சிவப்பாக மாற்றும்.
ஈ) அமிலங்கள் செயல்திறன் மிக்க உலோகங்களுடன் வினைபுரிந்து ஹைட்ரஜன் வாயுவைத் தருகின்றன.
உ) அயிலங்கள் உலோக கார்பனேட்டுகள் மற்றும் உலோக் பைகார்பனேட்டுகளுடன் வினைபுரிந்து கார்பன் டை ஆக்சைடைத் தருகின்றன.
சல்பியூரிக் அமிலம் வேதிப் பொருள்களின் அரசன் என்றழைக்கப்படுகிறது. ஏனெனில் பல சேர்மங்கள் தயாரிப்பதற்கு இது பயன்படுகிறது. வாகன மின்கலங்களிலும் இது பயன்படுகிறது. சிட்ரிக் அமிலம் உணவுப் பொருள்களைப் பதப்படுத்தப் பயன்படுகிறது. நைட்ரிக் அமிலம் உரமாகப் பயன்படும் அம்மோனியம் நைட்ரேட் என்ற டார்டாரிக் அமிலமானது ரொட்டிச் சோடாவின் ஒரு பகுதிப்பொருளாகும்.
ஊ ) அமிலங்கள் உலோக ஆக்சைடுகளுடன் வினை புரிந்து உப்பையும், நீரையும் தருகின்றன.
எ) அமிலங்கள் காரங்களுடன் வினைபுரிந்து உப்பையும் நீரையும் தருகின்றன
அமிலங்கள் பயன்கள்
உணவுப் பொருள்கள் கெட்டுப்போகாமல் இருக்க வினிகர் (அசிட்டிக் அமிலம் ) பயன்படுத்தப்படுகிறது.
ஊறுகாய் போன்ற உணவுப் பொருள்கள் கெட்டுப்போகாமல் இருக்க பென்சாயிக் அமிலம் பயன்படுத்தப்படுகிறது. பாலை
குளியல் சோப்புகள் மற்றும் சலவை சோப்புகள் தயாரிக்க உயர் கொழுப்பு அமிலங்களின் சோடியம் உப்புகள் அல்லது பொட்டாசியம் உப்புகள் பயன்படுகின்றன.
அனைத்து உயிரினங்களின் செல்களும் நியூக்ளிக் அமிலகளை அடிப்படைப் பொருளாகக் கொண்டுள்ளன. விலங்குகள் டி- ஆக்ஸிரிபோ நியூக்ளிக் அமிலத்தையும் (DNA) தாவரங்கள் ரிபோ நியூக்ளிக் அமிலத்தையும் (RNA) கொண்டுள்ளன.
ஹைட்ரோ குளோரிக் அமிலம், கழிவறைகளைத் தூய்மைபடுத்தும் பொருளாகப் பயன்படுகிறது.
சேர்மத்தையும், சாயங்கள் வண்ணப் பூச்சுகள் மற்றும் மருந்துகளையும் தயாரிக்கப் பயன்படுகிறது.
ஆக்ஸாலிக் அமிலம் குவார்ட்ஸ் படிகத்தில் ஏற்படும் இரும்பு மற்றும் மாங்கனீசு படிவுகளை சுத்தம் செய்யவும், மரப்பொருள்களைத் தூய்மையாக்கவும் மற்றும் கருப்புக்கறைகளை நிக்கவும் பயன்படுகிறது.
காரபானிக் அமிலம் காற்று அடைக்கப்பட்ட பானங்களில் பயன்படுகிறது.
அமிலக் கரைசலில் நீரின் பங்கு
அமிலங்கள் நீரில் கரையும் போது மட்டுமே தங்களின் பண்புகளை வெளிப்படுத்தும், நீரில் ஈரையும் போது ஹைட்ரஜன் (அயனிகளைத் தருவதால் அது அயிலம் என அறியமுடிகிறது. அதே சமயம் கரிமக் கரைப்பானில் அமிலங்கள் அயனியுறுவதில்லை.
வேதி வாய்ப்பாடு; 3 HCI + HNO
எடுத்துக்காட்டாக ஹைட்ரஜன் குளோரைடு நீரில் கரையும் போது H. அயனிகளைத் தருகிறது அதே சமயம் எத்தனால் போன்ற கரிமக் கரைப்பானில் அயனியறாமல் முலக்கூறுகளாகவே இருக்கும்
உலோகங்களில் தங்கம் மற்றும் வெள்ளி மட்டுமே HC மற்றும் HNO உடன் வினைபுரியாது என்பது நாம் அறிந்த ஒன்று ஆனால் இந்த இரண்டு அமிலங்களின் கலவை தங்கத்தைச் கரைக்கும் திறலுள்ளது அந்த கலவையின் பொயர் இராஜதிராவகம் எனப்படும்.
*இராஜதிராவகம் என்பது மூன்று பங்கு ஹைட்ரோகுளோரிக் அமிலம், ஒரு பங்கு நைட்ரிக் அமிலம் கலந்த கலவை ஆகும். இதன் மோலார் விகிதம் 3:1இது மஞ்சள் -ஆரஞ்சு நிறமுடைய புகையக்கூடிய திரவம் ஆகும். இது தங்கம் மற்றம் சில கடின உலோகங்களையும் அதிக அளவில் சரிமானம் செய்யக்கூடிய திறன் கொண்டது.
*இராஜ திராவகம் என்ற சொல் இலத்தீன் மொழியிலிருந்து பெறப்பட்டது. இதன் பொருள் திரவத்தின் அரசன் என்பதாகும். இது மிகுந்த ஆற்றல் கொண்டது இராஜதிராவகம் மிக உன்னதமான நிலையில் உள்ள தங்கம், பிளாட்டினம் மற்றும் பெல்லேடியம் போன்ற உலோகங்களைக் கூட கரைக்கவல்லது.
* இராஜதிராவகத்தின் பயன்கள்.
1. தங்கள் மற்றும் பிளாட்டினம் போன்ற உலோகங்களைத் கரைப்பதற்கு முதன்மையாகப் பயன்படுத்தப்படுகிறது.
2. தங்கத்தை சுத்தம் செய்யவும், சுத்திகரிக்கவும் பயன்படுகிறது.
What's Your Reaction?
 Like
0
Like
0
 Dislike
0
Dislike
0
 Love
1
Love
1
 Funny
0
Funny
0
 Angry
0
Angry
0
 Sad
0
Sad
0
 Wow
0
Wow
0